武汉康测科技有限公司
8 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0.2999999999999998
- 0.2999999999999998
- 1.2999999999999998
- 0.2999999999999998
公司新闻/正文
组蛋白修饰调控m6A修饰:METTL14抑制结直肠癌转移
3605 人阅读发布时间:2021-10-29 11:27

研究背景
我们知道,m6A修饰是真核生物mRNA中最为普遍的甲基化修饰,该修饰调控有以下三类蛋白参与:
- 甲基转移酶:METTL3、METTL14、WTAP等;
- 去甲基化酶:FTO、ALKBH5等;
- 甲基化阅读蛋白:YTHDF1/2/3、YTHDC1/2、IGF2BP1/2/3等;
1. 甲基转移酶METTL14在CRC中低表达,且与CRC进展相关
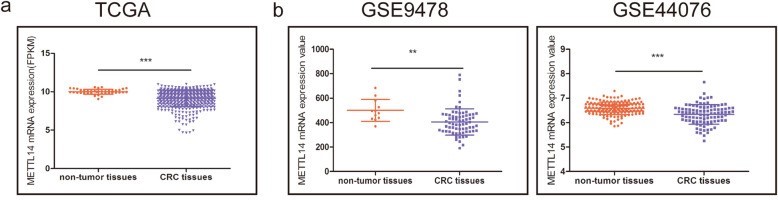
此后,作者对136例结直肠癌患者的癌组织、癌旁组织进行了qRT-PCR及IHC验证(下图c,d),结果与数据库中一致,癌组织中METTL14的表达明显降低。

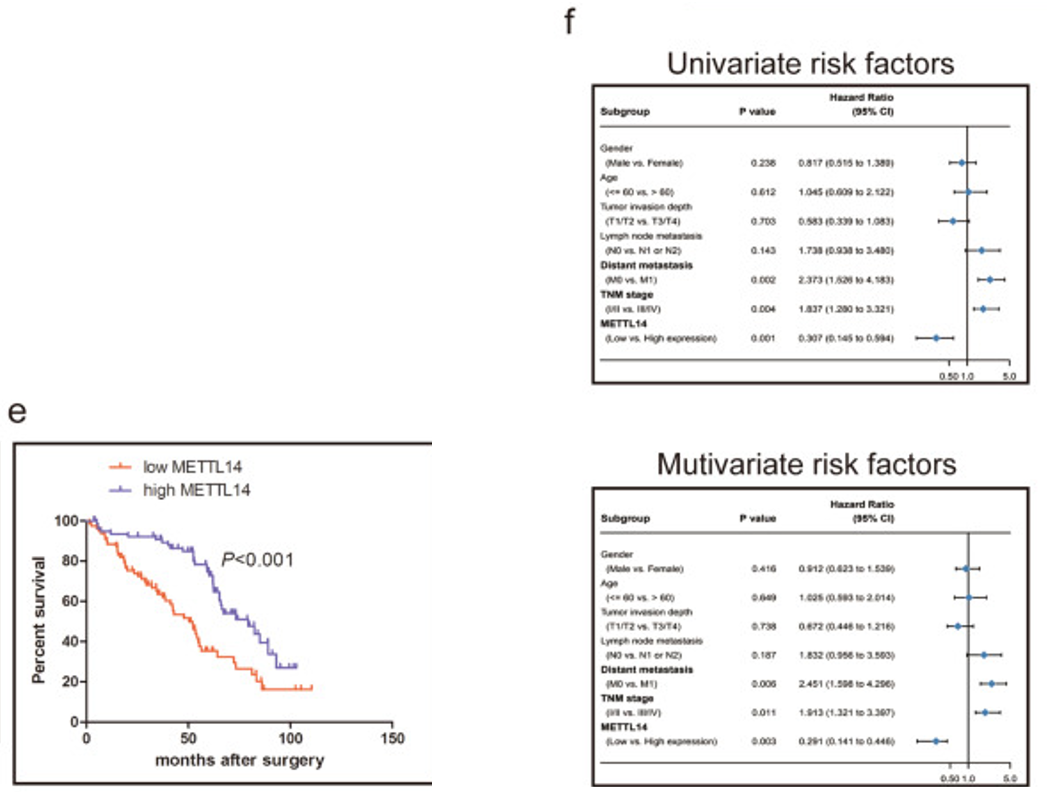
METTL14的低表达是否与CRC的致病进程有着某种联系呢?为了探究这一问题,作者接着进行了Kaplan-Meier生存分析,结果表明METTL14低表达的CRC患者总生存率(OS)较差(下图e)。不仅如此,METTL14的表达是OS的独立预后因素(下图f)。因此,癌组织中的METTL14低表达很可能与CRC的致病进程有着紧密联系。
2. KDM5C介导的H3K4me3去甲基化,抑制METTL14转录
CRC中METTL14低表达机制是什么?作者又在ENCODE数据库中查找了H3K4me3的ChIP-seq数据,发现CRC中METTL14启动子部位的H3K4me3修饰大幅降低(下图a)。
而据此前研究,KDM5C可介导H3K4me2/3的去甲基化,并抑制基因的转录,因此作者也关注了CRC中KDM5C的表达状况。与癌组织中的METTL14低表达相反,KDM5C的表达明显升高,暗示KDM5C与METTL14的表达负相关。
为了验证这一猜想,作者用KDM5C抑制剂处理了结直肠癌细胞系,经抑制剂处理后的细胞中METTL14的mRNA、蛋白水平均升高(下图b, c),敲低KDM5C的结果也一样(下图e)。
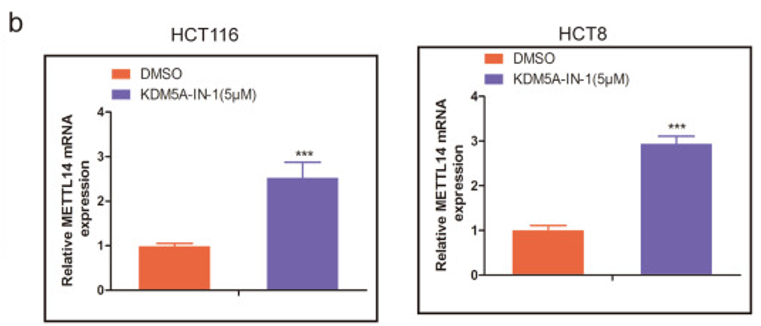
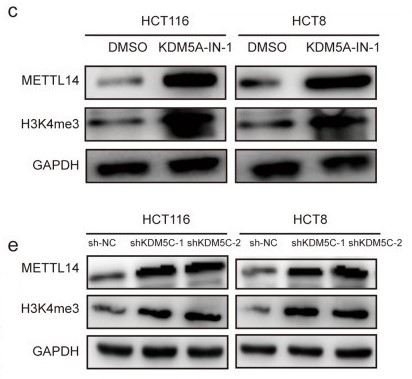
之后作者通过ChIP查看METTL14启动子区KDM5C的结合状况及H3K4me3的修饰水平,结果表明KDM5C的敲除增加了METTL14启动子区的H3K4me3修饰(下图f, g)。
综上,CRC中的KDM5C高表达,介导METTL14启动子区的H3K4me3修饰降低,从而抑制了METTL14表达。
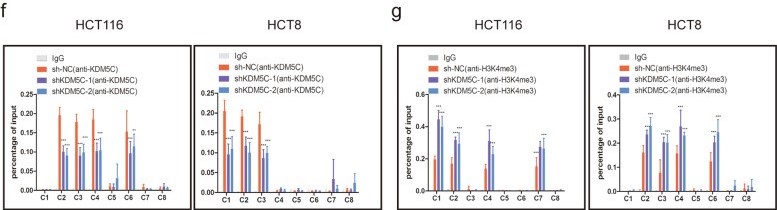
3. METTL14可抑制CRC的细胞迁移、侵袭及转移
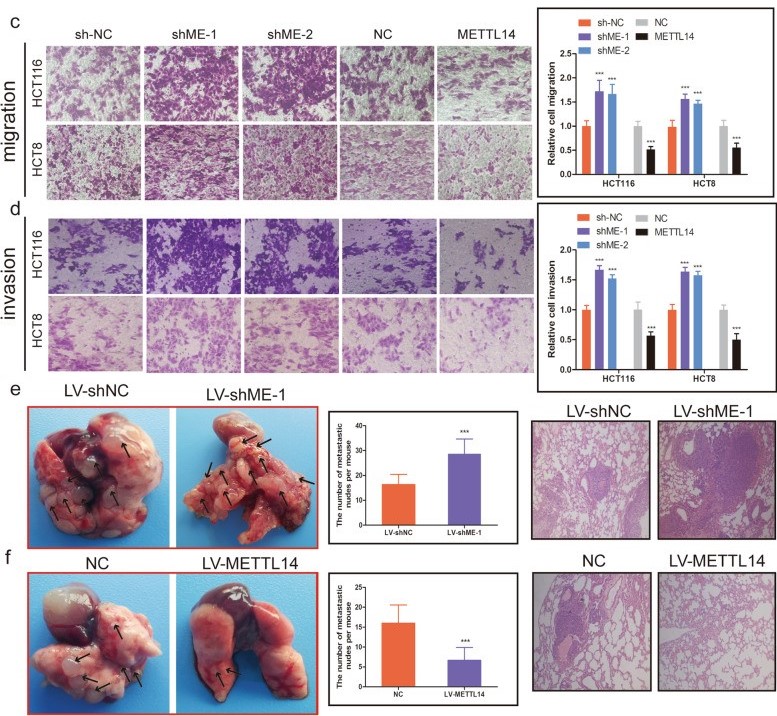
4. 甲基转移酶METTL14介导m6A修饰靶向SOX4
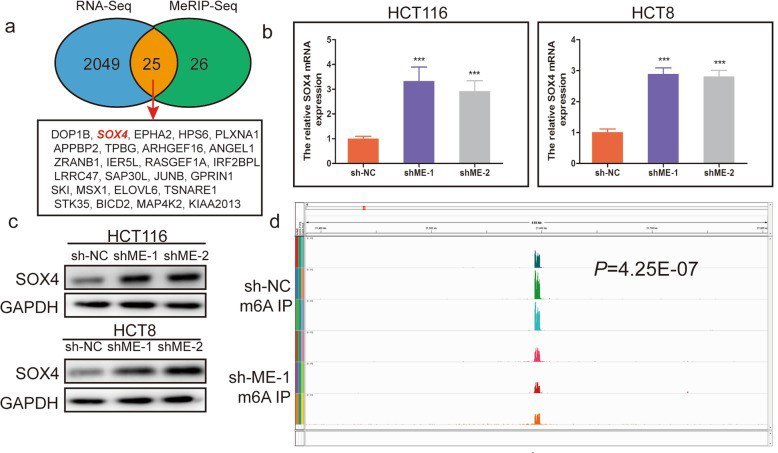
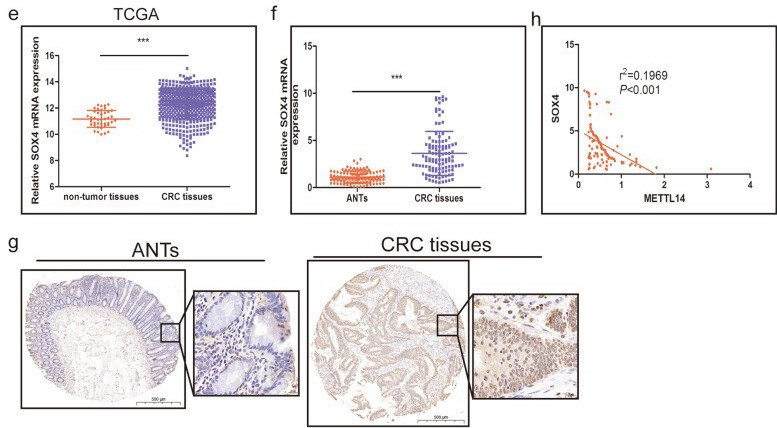
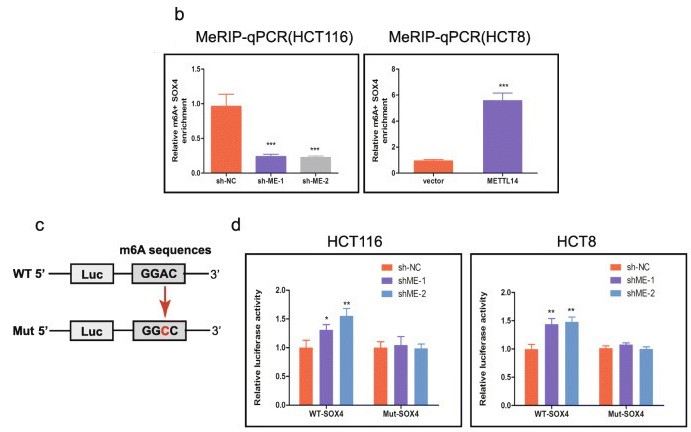
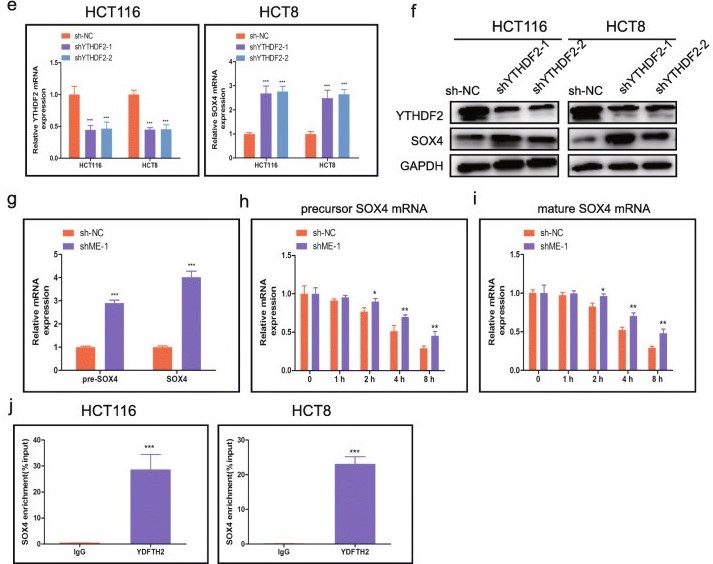
5. SOX4作为关键靶标,促进CRC的致病
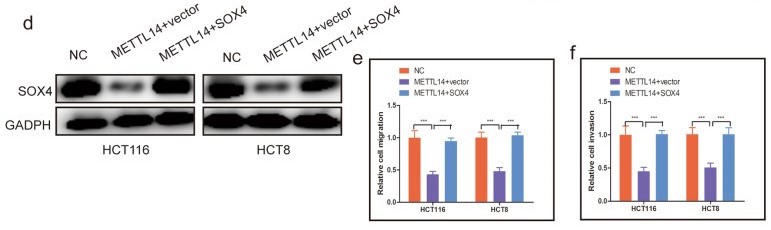
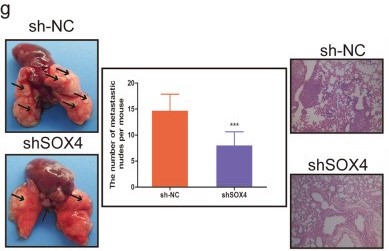
之前已发现METTL14与SOX4的表达负相关,过表达METTL14可抑制SOX4的表达,抑制细胞的迁移、侵袭;作者同时过表达METTL14和SOX4发现,SOX4过表达可以挽救因METTL14过表达而下降的细胞迁移、侵袭能力(下图d, e, f),且体内实验结果也与之一致,过表达SOX4使METTL14过表达小鼠体内的肺转移灶数目恢复至对照组水平(下图h)。上述结果表明,SOX4的确为METTL14下游的关键靶标,其表达可促进CRC的致病进程。


6. METTL14通过靶向SOX4,影响EMT和PI3K/Akt信号通路进而抑制CRC
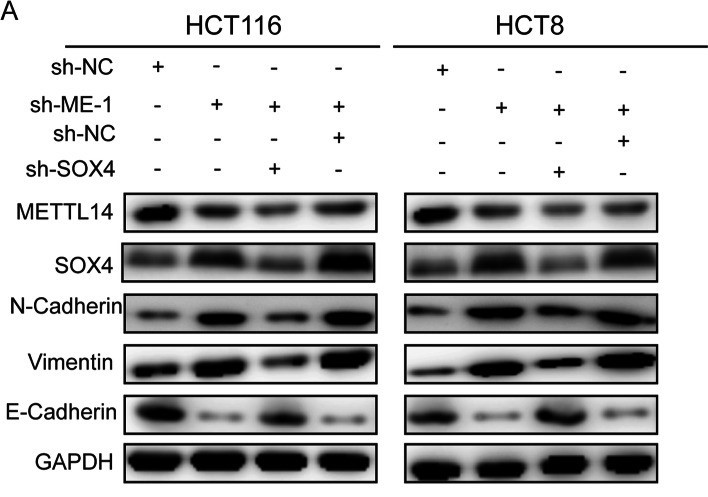
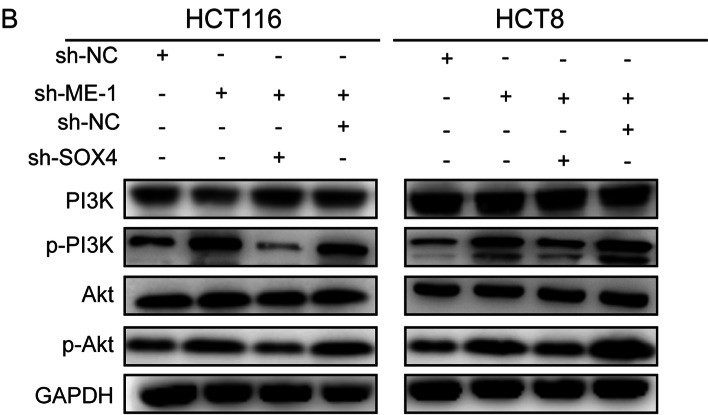
研究思路小结:
1. 首先探究某种疾病中m6A相关酶(如本文中的METTL14)是否表达异常;
2. 可选:寻找m6A相关酶(METTL14)编码基因上的组蛋白修饰变化;
3. 敲低/过表达相应基因(METTL14),探究m6A在该疾病中发挥的作用;
4. meRIP-seq、RNA-seq找到关键的靶标基因(SOX4);
5. 研究m6A调控靶标基因(SOX4)的机制,往往与甲基阅读蛋白(YTHDF2)相关;
6. 阐明靶标基因(SOX4)在该疾病中发挥的作用;
7. 对m6A相关酶-靶标基因(METTL14-SOX4)发挥的作用进行体内、体外实验验证。
这篇文献大体思路仍是m6A研究的经典思路,但作者在此基础上,还研究了上游组蛋白修饰对m6A相关蛋白(METTL14)的调控,给文章带来了新意。因此,m6A文章结合其他调控模式或许能更好的揭示调控机制,并获得更多的关注。参考文献:Chen, Xiaoxiang et al. “METTL14-mediated N6-methyladenosine modification of SOX4 mRNA inhibits tumor metastasis in colorectal cancer.” Molecular cancer vol. 19,1 106. 17 Jun. 2020, doi:10.1186/s12943-020-01220-7